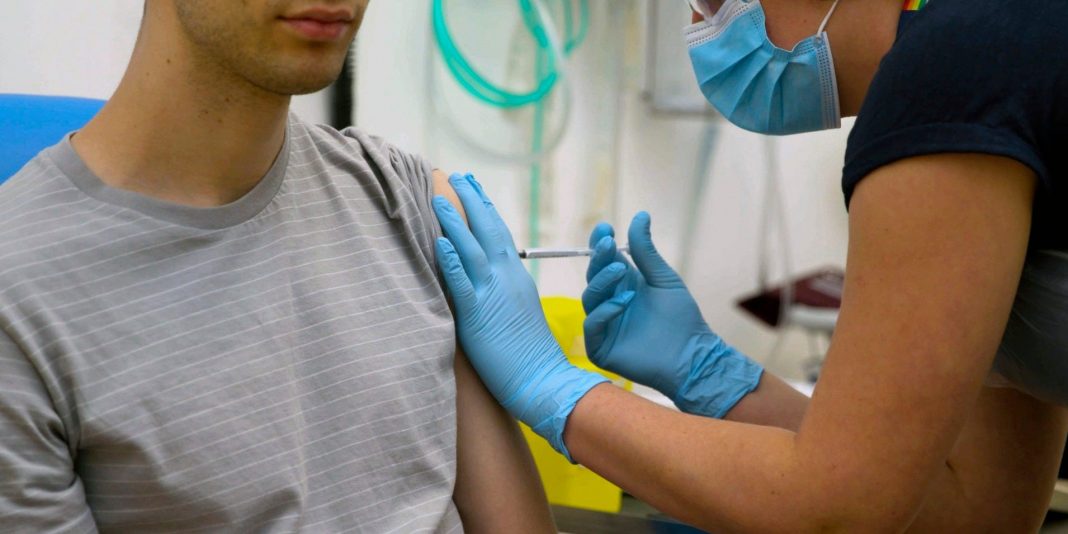
El primer ensayo clínico en nuestro país que probará una de las 4 vacunas más adelantadas para prevenir el coronavirus comenzará ahora en agosto. Los voluntarios se inscriben en una página web. Se trata del estudio de fase 3 de la vacuna del laboratorio estadounidense Pfizer y el alemán BioNTech, que en Argentina estará liderado por el infectólogo Fernando Polack. El ministro de Defensa, Agustín Rossi, confirmó que «ya se anotaron más de 15.000 voluntarios».
Indicó en un reportaje radial «se va a sumar personal del Hospital Militar que hará el seguimiento». (El Dr. Polack ya había revelado, en esta nota que publicó AgendAR, que el estudio de prueba de la vacuna contra la Covid-19 comenzaría en agosto en el Hospital Militar de la ciudad de Buenos Aires). Rossi sostuvo que hay voluntarios en las Fuerzas Armadas, pero los voluntarios ya anotados superan la necesidad prevista.
Esta vacuna ya tuvo buenos resultados en las primeras instancias de la investigación clínica. La fase 1 (donde se mide la seguridad) y fase 2 (donde se empieza a medir la eficacia) ya se están realizando en Estados Unidos y en Alemania, desde abril y mayo respectivamente. La fase 3 (confirmación de eficacia clínica, en una grupo humano mucho mayor) se hará en Estados Unidos, en Alemania, en Argentina. y probablemente en otros países, según anticipó Alejandro Cané, director de asuntos científicos de vacunas de Pfizer para Norteamérica.
En Argentina se probará el 20% del material disponible para esa etapa del ensayo. Para eso se reclutarán voluntarios de entre 18 y 85 años. No pueden participar mujeres embarazadas o en período de lactancia.
Quienes quieran sumarse a esta investigación, pueden expresar su voluntad en esta página web (verificada por la Administración Nacional de Medicamentos y Tecnología Médica (ANMAT). Esto fue necesario, porque para postularse al estudio hay que completar varios datos personales.
Desde la ANMAT aclararon que este organismo no participa en la convocatoria de voluntarios para los estudios clínicos ya que esto lo realizan los investigadores, en este caso la Fundación Infant, que lidera el doctor Polack. Lo mismo informaron desde la filial local de Pfizer.
Al ingresar a la página, lo primero con lo que se encuentra el interesado es una breve explicación sobre el estudio en la que se hace una aclaración importante: no todos los que finalmente sean seleccionados recibirán la vacuna.
«La mitad de los participantes en el estudio recibirá la vacuna en desarrollo y la mitad recibirá placebo –en forma de inyección de solución fisiológica. De esta manera se puede evaluar comparando los resultados en los dos grupos si la vacuna es eficaz para prevenir COVID-19. Esta división entre un grupo que recibirá el fármaco y otro que no (que se llama «grupo control») es el protocolo que se aplica en el estudio de todos los medicamentos.
El postulante tiene que completar un formulario, para que los investigadores puedan contactarse «y aclarar sus dudas».
Primero debe contestar tres preguntas: si tiene entre 18 y 85 años, si vive en CABA o a menos de 60 kilómetros de Capital y, si es mujer, si está embarazada o en período de lactancia.
Luego, si el postulante califica para el reclutamiento, tiene que informar su nombre, DNI, edad, dónde vive, y brindar también un e-mail, un celular y otro número de teléfono y un horario de contacto, además de responder a través de qué medio se enteró del proyecto. Finalmente, para completar el registro, tiene que validar la postulación a traves de un enlace que recibe por mensaje de texto en el celular que informó.
Desde la Cámara Argentina de Especialidades Medicinales (CAEME) emitieron esta semana un comunicado brindando detalles de cómo es la participación en una investigación clínica, que siempre es voluntaria y gratuita. El voluntario debe brindar su consentimiento a través de un proceso que incluye recibir información detallada de todo lo relacionado con la investigación. En cualquier momento puede cambiar su deseo de participar, sin consecuencias, y debe recibir toda nueva información obtenida sobre el producto en investigación. En todo estudio existe además un comité de ética que tiene como objetivo proteger los derechos y seguridad de los participantes.